
Kadmijum: hemijske štetnosti i uticaj na životnu sredinu Pregled
Семинарски рад
из предмета: ХЕМИЈСКЕ ШТЕТНОСТИ
Тема:
КАДМИЈУМ
Студент:
Нешковић Владимир
Шабац, март 2011.год.
САДРЖАЈ
УВОД.........................................................................................................1
ХЕМИЈА КАДМИЈУМА.......................................................................2
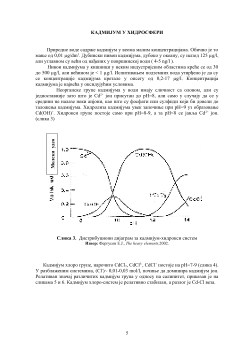
КАДМИЈУМ У ХИДРОСФЕРИ...........................................................5
КАДМИЈУМ У СЕДИМЕНТИМА.......................................................8
КАДМИЈУМ У ЗЕМЉИШТУ...............................................................8
КАДМИЈУМ У ОРГАНИЗМУ ЧОВЕКА.............................................9
ОПАСНОСТ ПО ЗДРАВЉЕ..................................................................10
МЕТОДЕ АНАЛИЗЕ...............................................................................12
ЗАКЉУЧАК…..........................................................................................13
ЛИТЕРАТУРА..........................................................................................14
1
ХЕМИЈА КАДМИЈУМА
Хемија кадмијума је у великој мери слична хемији цинка, међутим, док је цинк
важан есенцијални микроелемент, кадмијум је познат више по токсичности и
метаболичном антагонизму са цинком и другим елементима. Основна разлика у
хемији ова два елемента лежи у базности оксида, одн. хидроксида, који код
кадмијума скоро да немају кисела својства. Ипак у воденим растворима јона Cd
2+
долази до хидролизе, али је она знатно мење изражена него код цинка.
Највећи број једињења кадмијума припада степену оксидације +2, мада се у
ограниченом броју случајева јавља у једињењима степена оксидације +1. Раствара се
у киселинама (теже у неоксидирајућим, а лакше у киселинама које имају
оксидационо деловање), али не и у базама.
По заступљености у земљиној кори налази се на 67. месту са просечном
концентрацијом од 0,1 mg/kg. Незагађена земљишта обично садрже мање од 0,5
mg/kg кадмијума, а уобичајене вредности се крећу од 3 mg/kg, у зависности од
подлоге. Просечна концентрација кадмијума у земљиној кори креће се између 0,1-0,5
mg/kg. Веће концентрације се могу пронаћи у седиментним стенама. У морским
фосфатима и фосфоратима утврђене вредности су преко 500 mg/kg.
У природи се јавља углавном као редовни пратилац руда бакра, олова и цинка, у
којима се јавља као сулфид или карбонат. За индустријску употребу, кадмијум се не
екстрахује из руда, јер се довољне количине добијају у процесу топљења руде цинка,
сфалерит ( ZnS ), у којој је присутан CdS у значајним количинама.
Захваљујући специфичним физичким и хемијским особинама кадмијум има
широку употребу у производњи боја, легура, облога за делове од алуминијума или
челика у циљу повећања отпорности према корозији. Кадмијум се може наћи у
већим количинама поред путева, услед трошења аутогума и цурења аутомобилског
уља.
Присутан је у атмосфери, земљишту и водама, а повишене концентрације могу
изазвати озбиљне последице код свих живих организама. Нема никакве есенцијалне
биолошке функције, али је ипак пронађен у више од 1000 врста терестричне и
аквастичне флоре и фауне.
Количина кадмијума у отпадним водама је обично мала, али с обзиром да је врло
токсичан елемент, познат по концентрисању у живим организмима, потребно је
одредити и његову минималну концентрацију.
У природу доспева, распадањем стена, ерозијом, путем ветра, вулканске емисије,
шумских пожара, као и из антропогених извора из индустрије за прераду сировина,
саобраћаја, спаљивањeм фосилних горива, производњом цемента, комуналног
отпада и муља и истрошених батерија које се одбацују као отпад. У сеоским
подручјима кадмијум је у концентрацијама <0,5 ng/m
3
, a oko 50 ng/m
3
у
индустријским зонама.
У западним земљама фосфатна ђубрива су највећи антропогени извор кадмијума
са 58%, затим атмосферски гасови са 38-41% и канализациони муљ са 2-5%. Стајско
ђубриво садржи 0,3-1,8 mg/kg Cd у сувој материји. У Европи фосфатна ђубрива
производе око 300t Cd/год.
Биогеохемијски циклус и флуксеви кадмијума на површини земље
представљени су на слици 1
.
Подаци се односе на природне системе, међутим у
неким ситуацијама дата су два опсега концентрација.
2
Слика 1.
Биогеохемијски циклус кадмијума
Извор
: Фергусон Е.Ј.,
The heavy elements
,2002.
АТМОСФЕРА
БИОСФЕРА
Групе: Cd
2+
честице које садрже Cd
Концентрација:
0,003-20 ng/m
3
Таложење:
5,7x10
6
kg/год.
Таложење:
2,4 x10
6
kg/год.
Групе:
Cd
2+
, Cd-S-R
Групе: CdS, CdO,
CdCO
3
, Cd
2+
Групе: Cd
2+
,
CdCl
2
, Cd(OH)
+
,
CdCO
3
, CdSO
4
,
Cd-oрг., Cd-S-R
У земљишту:
0,01-500 µg/g
У стенама:
средња вредност
0,11 µg/g
Ерозија,
поплаве
2,2x10
6
kg/год.
У океанима:
<0,001-10 µg/l
Честице: 0,1-2 ng/l
У свежој води:
<0,01-50 µg/l
Концентрација:
0,01-2,5 µg/g (природно)
0,2-40 µg/g
(контаминирано)
Групе: CdS, CdO, CdCO
3
, Cd
2+
Концентрација: 0,01-50,000 µg/g
ЛИТОСФЕРА
ХИДРОСФЕРА
СЕДИМЕНТ
И
3
Želiš da pročitaš svih 16 strana?
Prijavi se i preuzmi ceo dokument.
Slični dokumenti

Ovaj materijal je namenjen za učenje i pripremu, ne za predaju.


























































