Povećanje mišićne mase Pregled
Завршни рад
Тема:
Повећање мишићне масе
Предмет:
Ментор: Студент:
Проф. др
Новембар, 2022. године
Апстракт
Инзулинска резистенција скелетних мишића је предиктор развоја дијабетеса типа 2 и
одржавање адекватног одлагања мишићне глукозе у мишићима може помоћи у
превенцији дијабетеса. Липодистрофија је врста дијабетеса узрокована смањењем белог
масног ткива и адипокина лептина. Као последица тога развијају се липидемија,
инсулинска резистенција и хиперфагија. У недавној студији, показали смо да повећање
скелетне мишићне масе инхибицијом сигнализације миостатина, члана породице
трансформишућег фактора раста β (ТГФβ) који негативно регулише раст мишића,
спречава развој дијабетеса у мишјем моделу липодистрофије. Инхибиција миостатина
специфична за мишиће такође је спречила хиперфагију што сугерише да мишићи могу
регулисати унос хране. Овде разматрамо ове резултате у контексту стратегија за
повећање осетљивости мишића на инсулин, као и нова открића о ефектима миостатина
и других чланова породице ТГФβ на сличне метаболичке процесе.
Кључне речи:
Инзулинска резистенција, скелетних мишића, мишићне глукозе,
дијабетес
Abstract
Skeletal muscle insulin resistance is a predictor of the development of type 2 diabetes, and
maintaining adequate muscle glucose disposal may help prevent diabetes. Lipodystrophy is a
type of diabetes caused by a decrease in white adipose tissue and the adipokine leptin. As a
consequence, lipidemia, insulin resistance and hyperphagia develop. In a recent study, we
showed that increasing skeletal muscle mass by inhibiting myostatin signaling, a member of
the transforming growth factor β (TGFβ) family that negatively regulates muscle growth,
prevents the development of diabetes in a mouse model of lipodystrophy. Muscle-specific
inhibition of myostatin also prevented hyperphagia suggesting that muscle may regulate food
intake. Here, we discuss these results in the context of strategies to increase muscle insulin
sensitivity, as well as new findings on the effects of myostatin and other TGFβ family members
on similar metabolic processes.
Key words:
Insulin resistance, skeletal muscle, muscle glucose, diabetes

2
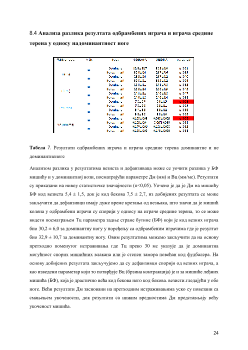
8.7 Анализа разлика резултата одбрамбених играча, играча средине терена и
нападача у односу на доминантну и не доминантну ногу ................................... 30
3
Увод
Скелетни мишићи су кључно ткиво за одржавање контроле глукозе у крви и енергетске
равнотеже. Мишићи користе и глукозу и масне киселине као гориво и служе као извор
аминокиселина за коришћење горива од стране других ткива током гладовања. Унос
глукозе у мишиће стимулише се контракцијом или секрецијом инсулина након оброка.
Студије еугликемијско-хиперинсулинемичне стезаљке код људи показују да се већина
инсулином стимулисаног преузимања глукозе у целом телу дешава у скелетним
мишићима где се највећи део складишти као гликоген или оксидује.
Интрамиоцелуларна акумулација липида је у корелацији са инсулинском резистенцијом
и детектује се много раније него почетак дијабетес мелитуса типа 2 (Т2ДМ). Прецизна
улога оксидације митохондријалних липида у патогенези мишићне инсулинске
резистенције се још увек расправља. Предложени су различити и потенцијално
преклапајући механизми за узрок акумулације липида, укључујући митохондријалну
дисфункцију која доводи до липотоксичности и инсулинске резистенције, непотпуну
оксидацију липида која доводи до штетних интермедијарних метаболита, или промене у
сигнализацији липида, редокс равнотежу или ЕР стрес.
Занимају нас метаболички ефекти члана породице трансформишућег фактора раста β
(ТГФβ) који негативно регулише раст скелетних мишића, миостатина (МСТН), посебно
у погледу прогресије, превенције или лечења уобичајених метаболичких стања. Недавно
смо објавили студију која описује превенцију дијабетеса и хиперфагије (прекомерног
уноса хране) код дијабетичких мишева са липодистрофијом, болешћу узрокованом
недостатком белог масног ткива (ВАТ), блокирањем сигнализације МСТН у мишићима.
Наши резултати се слажу са растућом спознајом да хипертрофија мишића има
благотворне ефекте на метаболизам глукозе и може такође да имплицира скелетне
мишиће у регулацији уноса енергије неким још непознатим механизмом. Овде ћемо
ставити наше резултате у контекст са неким тренутним активним областима
истраживања метаболичке хомеостазе.
До сада, за разлику од модела са повећаном оксидацијом липида у мишићима,
хипертрофични модели су доследно показивали побољшану осетљивост на инсулин или
метаболизам глукозе, посебно када мишићи претходе метаболичком изазову.
5
Код људи, чиста маса је позитивно повезана са смањеном инциденцом инсулинске
резистенције или метаболичког синдрома, групе фактора ризика за кардиоваскуларне
болести и Т2ДМ који укључује повишене нивое глукозе и триглицерида наташте,
хипертензију, гојазност и смањен ХДЛ. Попут вежби издржљивости, вежбе отпора су
такође повезане са побољшањем метаболизма глукозе и обе се сада препоручују за
пацијенте са Т2ДМ. Генетски модификовани мишеви са повећаном мишићном масом
имају смањену масу масног ткива и отпорност на гојазност изазвану исхраном (ДИО) и
инсулинску резистенцију чак и када манипулација је специфична за мишиће.
Једно од објашњења за ово може бити да сигнализација инсулина и фактора раста
сличног инсулину 1 (ИГФ1) конвергира на фосфатидил инозитол (ПИ) 3-
киназу/Акт/сисарску мету рапамицина (мТОР) пут за промовисање одлагања глукозе
стимулисане инсулином и анаболичког раста у мишићима. Дакле, сигнални путеви који
промовишу мишићну хипертрофију су потенцијалне мете за миметике вежбања отпора
који могу имати додатну корист од спречавања или лечења мишићне инсулинске
резистенције.
Аналогно адипокинима који се излучују из масних ћелија, мишић се све више препознаје
као секреторно ткиво које производи потенцијално стотине сопствених „миокина“ који
могу деловати локално или системски. Неки од њих се повећавају вежбањем и могу
посредовати у ефектима вежбања на друге марамице. На пример, како су недавно
описали Спиегелман и колеге, ирисин из мишића промовише диференцијацију смеђег
масног ткива (БАТ) и термогенезу у ВАТ. Насупрот томе, експресија МСТН у мишићима
се често смањује вежбањем, али се повећава са инсулинском резистенцијом или
морбидном гојазношћу. Штавише, поновљено убризгавање МСТН може изазвати
интолеранцију на инсулин код мишева.
Губитак функцијских мутација у МСТН гену или третман растворљивим МСТН
антагонистима у великој мери повећава величину скелетних мишића.15 Делеција Мстн
гена или трансгена прекомерна експресија доминантног негативног активинског
рецептора типа ИИБ (АЦВР2Б, такође познат као АцтРИИБ) током развоја изазива
повећање мишића број влакана (хиперплазија) и пречник (хипертрофија) код мишева.
Мстн мутантни мишић код мишева или расе белгијске плаве говеда такође садржи више
брзих гликолитичких влакана од нормалних мишића.
2
2
Boyle, M. (2016): New functioanl training for sports. USA: Human Kinetics, стр. 52
Želiš da pročitaš svih 39 strana?
Prijavi se i preuzmi ceo dokument.
Slični dokumenti

Ovaj materijal je namenjen za učenje i pripremu, ne za predaju.