
Agregatna i fazna stanja kod polimera Pregled
Univerzitet u Nišu
Fakultet zaštite na radu u Nišu
Predmet: Tehnički materijali
SEMINARSKI RAD
Agregatna i fizička stanja kod polimera
Mentor: dr Dragan Mitić
Studenti: Martina Živković 12148
Asistent:mr Milan Protić Marko Jovanović 12106
Niš, 2014.
SADRŽAJ
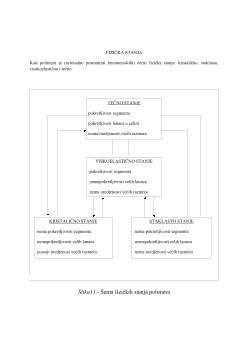
Agregatna i fazna stanja
Zavisno od stepena uredjenja dugolančanih makromolekula, kao i od spoljašnjih parametara
(temperature, pre svega), polimeri mogu biti u dva agregatna stanja: čvrstom ili tečnom. Čvrsto
agregatno stanje karakterišse se odredjenim dimenzijama i oblikom, u geometrijskom smislu. Ono
nastaje kada energija medjumolekulskog dejstva nadvlada energiju toplotnog kretanja molekula. Pod
dejstvom spoljašnjih sila oblik i zapremina se teško menjaju. Kod ovog agregatnog stanja rastojanja
izmedju molekula su mala (tzv. gusto pakovanje), uz oscilovanje molekula ili delova molekula oko
sopstvenih ravnotežnih položaja ( frekfencija oscilacilovanja je oko 10
13
-10
14
s
-1
) i bez translatornog ili
rotacionog kretanja. Tečno agregatno stanje karakteriše približna jednakost energije
medjumolekulskog dejstva i energije toplotnog kretanja molekula. Pod uticajem spoljasnjih sila
zapremina tečnosti se tesko menja, ali, za razliku od čvrstih tela, tečnosti lako zauzimaju oblik posude
u koju se sipaju. Gasovito agregatno stanje kod polimera nije zastupljeno jer, s obzorom na veliku
molekulsku masu u usled toga jake medjumolekulske inetakcije, pre nego što bi makromolekul mogao
preći u gasno stanje dolazi do njegove degradacije.
Ako se izvrše poredjenja svojstava supstanci u istom ili različitim agregatnim stanjima, ona ukazuju da
je podela na agregatna stanja nedovoljna za potpuno opisivanje tih svojstava. Prema tome, radi
potpunijegkarakterisanja polimera potrebno je, uz pojam agregatnog stanja, uvesti i pojam faznog
stanja.
Ukupan deo heterogenog sistema, homogen po hemijskom sastavu i fizičkom stanju, odvojen od
ostalih delova oštrim, jasno uočljivim granicama, sa mogućim razlikama u sastavu, strukturi i
termodinamičkim svojstvima, nezavisno od njegove mase, naziva se fazom. Faza treba da ima
dozvoljenu zapreminu da bi se moglo govoriti o pritisku, temperaturi i drugim termodinamičkim
svojstvima faze.
S obzirom na to da se polimeri mogu nalaziti u čvrstom agregatnom stanju, treba istaći da čvrstom
agregatnom stanju mogu odgovarati dva fazna stanja: kristalično i staklasto, a tečno fazno stanje može
da se nadje u dva agregatna stanja: staklastom i rastopu.
Pod dejstvom faznog prelaza podrazumeva se transformacija iz jedne faze u drugu, pri čemu dolazi do
promene u medjusobnom rasporedu molekula i termodinamičkih karakteristika supstance. Promena
medjusobnog rasporeda molekula izaziva promenu entropije u sistemu ako se menja stepen
uredjenosti, odnosno zapremine ako se menjaju rastojanja, tj. stepen interakcija molekula u sistemu.
Poznato je da se fazni prelaz prvog reda definiše kao prvi izvod Gibsove slobodne energije G po
temperaturi, i predstavlja entropiju S, ili prvi izvod slobodnje energije po pritisku, koji predstavlja
zapreminu V. U tačkama faznog prelaza pokazuje se skokovita promena entropije i zapremine, tj.
postoji skok ΔS i ΔV vrednosti, pa će se, analogno tome, skokovito i entalpija sistema (ΔH):
Želiš da pročitaš svih 14 strana?
Prijavi se i preuzmi ceo dokument.
Slični dokumenti

Ovaj materijal je namenjen za učenje i pripremu, ne za predaju.


























































