Pirazin: struktura, dobijanje, reaktivnost, derivati i primena Pregled
S A D R Ž A J
Kondenzacijom 1,2-dikarbonilnih jedinjenja i 1,2-diamina.........................................5
Ovom reakcijom nastaje 2,3-dihidropirazin koji oksidacijom sa CuO ili MnO2 u
Kondenzacijom dva molekula α-amino-karbonilnih jedinjenja..................................5
Ovom reakcijom nastaje 3,6-dihidropirazin koji oksidacijom, uglavnom pod blažim
Retrosinteza pirazinskog sistema se zasniva se na principima koji važe i za ostale
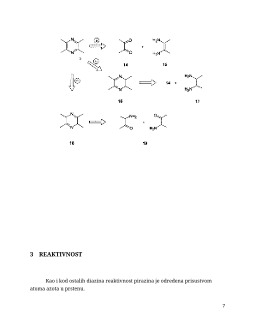
Pod običnim uslovima je otežana, dok prisustvo aktivirajućih grupa omogućava
1
U reakciji sa peroksidom nastaje N-oksid i jako lako N,N-dioksid..............................9
U prisustvu Na u vrelom etanolu dolazi do redukcije pirazina do piperazina..........9
Neki alkilprazini se pojavljuju u prirodi kao jako aromatične supstance koje često
Piperazin (heksahidroksipirazin) predstavlja osnovu grupe jedinjenja koja se
Hinoksalin (benzo[b]pirazin) je heterociklično jedinjenje koje sadrži kompleksni
Fenazin (benzo[b]hinoksalin) je dibenzopirazin koji predstavlja početnu supstancu
2
Elektronska struktura
1.2 Nomenklatura
Naziv pirazin su 1887. godine, nezavisno jedan od drugog, predložili Mason i Volf
(Wolff) kako bi pokazali analogiju sa piridinom, međutim iste godine Knor
( Knorr) je upotrebio ovaj naziv za pirol tetrahidrid, dok su Braun i Majer (Meyer)
za ovo jedinjenje predložili naziv aldin. Pošto je utvrđena sistematična
nomenklatura za azine, pa tako i za diazine, naziv pirazin je konačno prihvaćen
za ovo jedinjenje.
Pored ovih naziva za ovo jedinjenje koriste se još i 1,4-diazabenzen, p-diazin, 1,4-
diazin, paradiazin, piazin.
1.3 Fizičko-hemijske osobine
Pirazin je belo kristalno aromatično jedinjenje, tačka topljenja ovog jedinjenja je
52
○
C, a tačka ključanja 115
○
C.
Pirazin je vrlo slaba baza sa pKa= 0.6 što ga čini najslabijom bazom među
diazinima. Takođe za razliku od ostalih diazina on ima sposobnost građenja
relativno stabilnog anjona.
4
Želiš da pročitaš svih 14 strana?
Prijavi se i preuzmi ceo dokument.
Slični dokumenti

Ovaj materijal je namenjen za učenje i pripremu, ne za predaju.