Alkoholi: maturski rad iz hemije Pregled
Zrenjaninska gimnazija
Zrenjanin
MATURSKI RAD
Oblast: Hemija
Tema: Alkoholi
Profesor-mentor: Ucenik:
Lolita Uzelac Jelena
Pivarski
0
Zrenjanin
Jun, 2012.
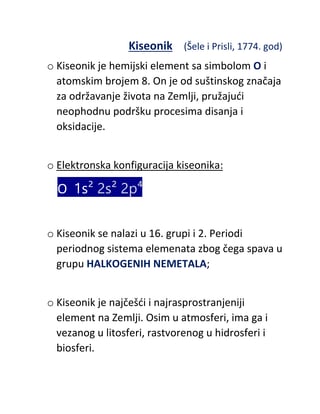
Alkoholi
Alkoholi su derivati ugljovodonika, koji u svom molekulu sadrze
hidroksilnu
(-OH) grupu
, vezanu za ugljovodonični ostatak koji može biti: zasićen,
nezasićen, aromatičan, supstituisan i dr.
Hidroksilna (-OH) grupa
Alkoholi sadrže polarnu –OH grupu. Kiseonik iz ove grupe je parcijalno
negativan (δ-), vodonik je parcijalno pozitivan (δ+).
Ovakva veza se naziva
polarizovanom ili polarnom vezom.
Kada se parcijalno negativan kiseonik jednog molekula dovoljno približi
parcijalno pozitivnom vodoniku drugog molekula, dolazi do
elektrostatičkog
privlačenja
tj. formiraju se
vodonične veze
, usled čega se molekuli asosuju.
Vodonična veza predstavlja jaku međumolekulsku interakciju.
Energija vodonične vetze iznosi 10-40 KJ/mol, sto je dovoljno da utiče na
osobine jedinjenja.
Zbog svoje polarnosti, -OH grupa utiče na reakcije alkohola, pa prema tome
alkoholi mogu da reaguju dvojako:
1. Može da dodje do raskidanja -O-H veze sa izdvajanjem protona (kiselost
alkohola)
2. Može da dodje do raskidanja -C-O veze pri čemu dolazi do supstitucije -
OH grupe.
Dokaz strukture alkohola
Hidroksilna grupa se može dokazati na osnovu dve reakcije:
1

2-butanol
izo-butil-alkohol
2-metil 1-propanol
sec-butil-alkohol
2-metil 2-propanol
t-butil-alkohol
Podele alkohola
Prema R-ostatku, alkoholi se dele na:
1.
Zasićene
-R: ( -CH
3
; -C
2
H
5
… )
2.
Nezasićene
-R: ( -CH
2
=CH-CH
3
… )
3.
Aromatične
-R: (
;
…)
Prema strukturi C-atoma, alkoholi se dele na:
1. Primarne - 1°
2. Sekundarne - 2°
3
3. Tercijarne - 3°
Prema broju –OH grupa, alkoholi se dele na:
1. Monohidroksilne
2. Dvohidroksilne
3. Polihidroksilne
Monohidroksilni alkoholi
Nalaženje i dobijanje alkohola:
Alkoholi su jedinjenja koja su veoma rasprostranjena u prirodi. Nalaze se ili
kao slobodni ili u vezanom obliku, kao estri (masti, voćne esencije, voskovi…)
Alkoholi se mogu dobiti na sledeće načine:
1.
Adicijom vode na alkene u prisustvu sumporne kiseline
U zavisnosti od toga da li želimo da dobijemo primarni, sekundarni ili
tercijarni alkohol, voda se adira na različite alkene (eten, propen i 2-
metil- propen)
4
Grinijarova reakcija sa aldehidima i ketonima predstavlja vrlo efikasnu
metodu za dobijanje složenijih alkohola. Grinijarov reagens (RMgX) sa
formaldehidom gradi primarne alkohole, sa drugim aldehidima gradi
sekundarne alkohole a sa ketonima gradi tercijarne alkohole.
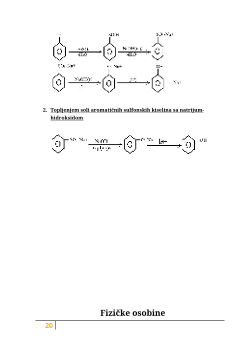
5. Hidrolizom estara
Hidroliza se može vršiti pomoću kiselina i alkalija.
U zavisnosti da li se vrši sa kiselinom ili bazom, proizvod reakcije je
alkohol i kiselina, odnosno so kiseline.
Fizičke osobine
Zbog vrlo polarne hidroksilne grupe, niži alkoholi se rastvaraju u vodi.
Rastvorljivost se objašnjava prisustvom vodoničnih veza između molekula
alkohola i molekula vode. I molekuli alkohola međusobno asosuju, tj.vlada
intermolekulska vodonična veza, pa su zbog toga njihove tačke ključanja
znatno više u odnosu na tačke ključanja odgovarajućih ugljovodonika.
Niži alkoholi su lako pokretljive tečnosti, a viši su uljaste ili čvrste supstance.
6
Želiš da pročitaš svih 30 strana?
Prijavi se i preuzmi ceo dokument.
Slični dokumenti

Ovaj materijal je namenjen za učenje i pripremu, ne za predaju.